-
行业和服务
- 电器
- 暖通空调制冷
- 照明
- 水和管道
-
技术和电子产品
-
消费类电子产品
-
5G 合规性测试
-
5G 射频测试与合规认证
-
EMC 电磁兼容预认证测试
-
FCC 测试与认证
-
IEC 62368-1 测试和认证
-
Matter 测试及认证服务
-
OCF(开放互联论坛)认证测试
-
SAR测试服务
-
Wi-Fi 测试和认证
-
Zigbee 认证和互操作性测试
-
光辐射测试和评估服务
-
增强现实、虚拟现实和混合现实测试与认证
-
无线射频产品的 EMC 测试和认证
-
无线射频产品的无线射频测试和认证
-
无线设备的测试和认证解决方案
-
消费和商用机器人
-
物联网测试服务
-
物联网设备开发的五大挑战
-
物联网设备的Thread认证测试
-
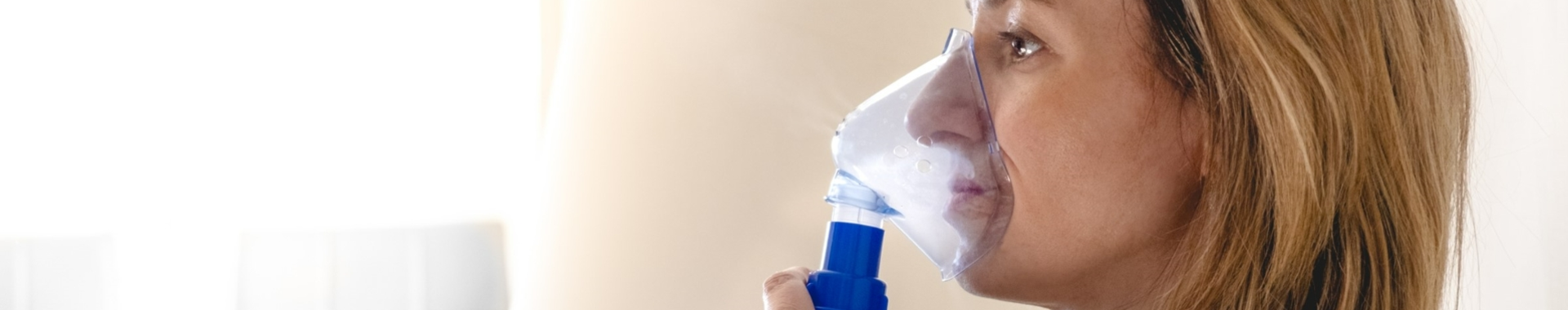
电子烟及雾化设备的电池和电气安全认证
-
能效检测和认证
-
蓝牙联盟资格测试与认证服务
-
5G 合规性测试
- 信息和通信技术
-
消费类电子产品
- 电池和组件
- 医疗保健和生命科学
- 汽车和移动出行
-
零售和消费品
-
建筑与施工
-
能源和公用事业
- 工业产品和系统
- 化学品和材料
-
电线和电缆
- 金融和投资服务
- 其他服务
- 软件服务
- 新闻
- 活动
- 关于我们
- 支持中心
搜索
热门搜索词
- 检测认证
- 应用安全科学
- UL认证
- 全球市场准入
软件服务
![Solutions]()
利用我们对安全、安防和可持续发展的战略性解决方案,助力您自信地进行创新,以应对纷繁复杂的商业挑战。

Next
Previous
新闻
关于我们
![关于UL]()
作为全球应用安全科学专家,我们助力客户创新,推出新产品和服务,驾驭全球市场和复杂的供应链,并以可持续和负责任的方式走向未来。

Next
Previous
活动
支持中心
我们是全球安全科学的专家
作为应用安全科学的全球专家,UL Solutions将产品安全、信息安全和可持续性挑战转化为100多个国家/地区的客户的机遇。UL Solutions提供测试、检验和认证服务以及软件产品和咨询服务,以支持我们客户的产品创新和业务增长。
了解我们的行业和服务
-


电器
-
暖通空调制冷
-


照明
-

水和管道
-


技术和电子产品
-


电池和组件
-

医疗保健和生命科学

医疗保健和生命科学
-

汽车和移动出行
-

零售和消费品
-

建筑与施工

建筑与施工
-

能源和公用事业
-

工业产品和系统
-

化学品和材料
-

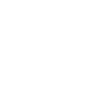
电线和电缆
-
金融和投资服务
金融和投资服务
-

其他服务
最新活动
新闻动态
在全球40+国家和地区
-
我们拥有
15000+
员工
-
我们设有
150+
分支机构
-
我们创立了
90+
实验室
-
我们的客户来自于
100+
国家和地区
-
全球有
数十亿
产品上出现UL标志
-
我们合作和服务于
60%+
全球500强和财富500强公司
-
我们是全球
1300+
标准和技术委员会成员
-
我们的软件服务于
21000+
来自各行各业的组织和机构
客服
微信客服